CFDAとは?
中国市場にて医療機器、医薬品、医薬品包材、化粧品、保健食品を販売するための要件、中国の強制登録。
日本国に於ける製造販売承認書に相当する厚生労働省認証に相当。米国のFDAによるPMA認証、欧州のCE認証に準ずる)
中国CFDA登録の特徴
| 対象区分 | 医療機器の場合、第一類、第二類、第三類 他の品目の場合、そのような区分無し |
|---|---|
| 再登録制 | 登録証には有効期限の設定 (品目によって 4年または5年、但し期間延長の可能性)登録の維持・継続には有効期限までに登録更新が必要 |
| その他 | 日本のような現登録に対する微細変更・追加“一変”が 受け入れられず、その場合 次の再登録に織り込む |
登録に要する期間は?
医療機器の場合 その期間に大きなバラツキ認められるも、目安としては
○ 第一類約7カ月
○ 第二類、第三類約15カ月
<注>・第一類、臨床試験、タイプ試験、いずれも実施不要
・第二類、第三類は タイプ試験の実施要
・中国側臨床試験(治験)は 次の場合に免除の可能性あり
① 日本厚生労働省「製造販売承認書」または米国FDA「PMA(又は510K)証書」等のいずれかの取得済みの 申請者に対して
② 既にCFDA登録実績が有れば、第二類製品、第三類製品の登録に対して
・ 初めて、第二類製品、第三類製品をCFDA登録申請する者に対しては
上記①であっても臨床試験要求される可能性あり
●化粧品の場合、普通化粧品、特殊化粧品の別により5カ月~8カ月
●保健食品、医薬品、医薬品包材の場合、2年以上
●バラツキとは 申請者保有の資料/Dataの的確性および完成度による。 但し、申請者/申請代行者間の 密なる意思疎通と協力関係によっては期間短縮への可能性を含む。
医療機器の中国CFDA登録手順とは?
Class I
準備 (1. 書類翻訳、2. 製品標準の作成、3. 登録関連書類の準備)
書類審査
登録証取得
Class II
準備 (1. 書類翻訳、2. 製品標準の作成)
製品試験検査
(臨床試験 ※人体注入型等)
(工場審査 ※人体注入型等)
登録書類準備
書類審査
登録証取得
医薬品の中国CFDA登録手順とは
化粧品の中国CFDA登録手順とは?
中国の化粧品は「特殊用途化粧品」と「非特殊用途化粧品」に分けられています。
「特殊用途化粧品」:育毛用、ボディケア用、バスト美容用、ヘアカラー用、パーマネン ト用、日焼け止め、消臭用、シミ取り用、脱毛用、9種類があり ます。
「非特殊用途化粧品」:ヘアケア、スキンケア、メークアップ、ネイルケア、芳香、5 種 類があります。
日本の医薬部外品は特殊化粧品か薬品になる可能性がありますので、化粧品の成分表、 品質基準、パッケージを確認後に判断致します。
1、「特殊用途化粧品」の登録申請手順:
サンプル検査→申請資料確認→CFDA 受理センターに提出し審査→CFDA 審査委 員会による技術評価審査(月に一回)→CFDA 薬品化粧品注冊司による再審査→
「輸入化粧品衛生許可証」発行 2、「非特殊用途化粧品」の登録申請手順:
サンプル検査→申請資料確認→CFDA 受理センターに提出し審査→CFDA 専門家 による評価審査(随時)→CFDA 薬品化粧品注冊司による再審査→「輸入化粧品 衛生許可証」発行
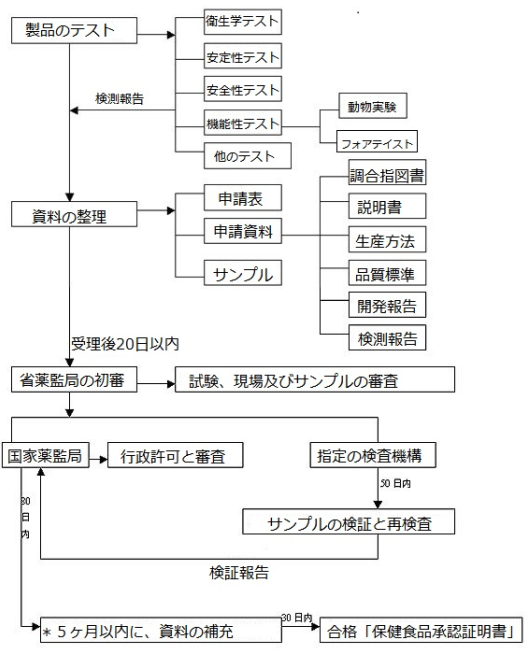
健康食品中国CFDA登録手順とは?